第三代试管婴儿:从实验室到临床的突破与伦理争议
自1978年世界首例试管婴儿诞生以来,辅助生殖技术经历了从体外受精到单精子注射的跨越式发展。1990年,英国科学家通过胚胎植入前遗传学诊断(PGD)技术,成功筛选出不含囊性纤维化致病基因的胚胎并移植,标志着第三代试管婴儿技术的正式诞生。这项技术通过基因检测手段,在胚胎植入前排除染色体异常或单基因遗传病,为遗传病高风险家庭提供了生育健康后代的希望。然而,随着技术从实验室走向临床,其引发的伦理争议也日益凸显。
技术突破:从“筛查”到“精准干预”的跨越
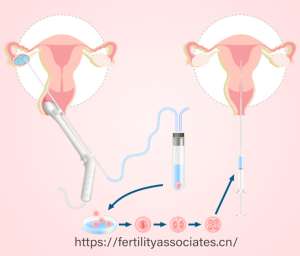
第三代试管婴儿技术的核心在于胚胎植入前遗传学检测(PGT)。早期技术受限于检测精度,仅能筛查染色体数目异常(如唐氏综合征)和少数单基因病(如地中海贫血)。随着二代测序(NGS)技术的普及,检测范围扩展至200余种单基因遗传病,并可识别染色体微缺失、微重复等复杂异常。例如,日本大阪大学医学部附属病院通过全基因组分析技术,将隐性遗传病阻断成功率提升至99.9%,使40岁以上患者胚胎着床率达到42%。
技术进步还体现在操作方式的革新。传统PGD需从胚胎中提取5-8个细胞,存在0.1%的损伤风险。2025年,日本英医院生殖中心研发的“NIPT-Embryo”技术,通过分析胚胎培养液中的游离DNA(cfDNA),实现了无创遗传学筛查,检测准确率达98.7%,且完全避免胚胎损伤。这一突破为高龄患者或珍贵胚胎的筛选提供了更安全的解决方案。
临床应用:从“解决生育难题”到“挑战生命伦理”
第三代试管婴儿技术的临床价值已得到广泛验证。在中国,河南省洛阳市妇幼保健院等机构通过PGT技术,帮助血友病、脊髓性肌萎缩症等遗传病家庭成功生育健康孩子。日本则通过技术普惠,将国际患者占比提升至35%,其中中国患者占比达60%,主要诉求包括高龄生育、遗传病阻断等。
然而,技术的临床应用也引发了多重伦理争议。生命权与选择权的冲突尤为突出:胚胎是否应被视为具有生命尊严的个体?淘汰异常胚胎是否构成“生命淘汰”?支持者认为,这是为了保障后代健康,符合“优利益原则”;反对者则强调,早期胚胎已具备发育为人的潜力,任何筛选都可能侵犯其生命权。
社会公平与基因歧视风险同样不容忽视。PGT技术的高昂费用(单周期费用约10万至30万元)使其成为“少数人的特权”。若技术被用于非医学目的的性别选择或“设计婴儿”,可能加剧社会不平等,甚至引发基于基因特征的歧视。例如,保险公司可能因个人基因信息拒绝承保,就业市场可能因基因缺陷排斥求职者。
家庭伦理与人口结构失衡也是争议焦点。技术可能改变传统家庭关系:若父母通过基因编辑选择胚胎特征,孩子可能被视为“定制产品”,影响亲子情感;若技术被用于性别选择,可能导致性别比例失衡,威胁社会稳定。
平衡创新与伦理:构建全球监管框架
面对技术争议,多国已出台监管措施。中国将辅助生殖技术纳入严格审批制度,仅允许省级卫生行政部门许可的机构开展PGT;日本生殖医学学会(JSRM)主导修订的《PGT技术临床应用指南》,将胚胎活检细胞数从5-8个减少至3-5个,以降低损伤风险;世界卫生组织(WHO)则采纳日本标准,将其作为全球生殖中心的操作规范。
未来,技术的可持续发展需兼顾创新与伦理。一方面,应通过立法明确胚胎法律地位,禁止非医学目的的基因选择;另一方面,需建立普惠医疗机制,降低技术成本,避免其成为“富人游戏”。此外,加强公众伦理教育,引导社会形成对辅助生殖技术的理性认知,也是平衡技术进步与伦理风险的关键。
第三代试管婴儿技术是人类对抗遗传病的里程碑,但其发展始终伴随着生命伦理的拷问。从实验室到临床,技术的每一步突破都需在科学理性与人文关怀之间寻找平衡点。唯有如此,这项技术才能真正成为造福全人类的“生命礼物”。