遗传病家庭的“零风险”生育:三代试管PGT技术实战指南
对于携带遗传病基因的家庭而言,生育健康后代曾是难以跨越的障碍。随着三代试管婴儿技术(PGT)的成熟应用,通过胚胎植入前遗传学检测阻断致病基因传递,已成为实现“零风险”生育的核心解决方案。本文将从技术原理、适应症、操作流程及实战案例四方面,为遗传病家庭提供系统性指南。
一、技术原理:基因层面的精准“排雷”
PGT技术通过在胚胎移植前对遗传物质进行检测,筛选出未携带致病基因的健康胚胎。其核心流程包括:
胚胎培养:将受精卵培养至囊胚期(第5-6天),此时胚胎已分化为滋养层细胞(未来发育为胎盘)和内细胞团(未来发育为胎儿)。
活检取样:通过微创技术提取滋养层细胞,避免损伤内细胞团。
基因检测:采用二代测序(NGS)技术,对胚胎的23对染色体进行全基因组分析,可检测出单基因突变、染色体非整倍体及结构异常。
以地中海贫血为例,若父母均为β-地贫基因携带者,传统生育方式下,子女有25%概率患重型地贫。而通过PGT-M(单基因病检测)技术,可精准筛选出未携带致病基因的胚胎,阻断疾病代际传递。
二、适应症:覆盖高风险生育场景
PGT技术适用于以下遗传病家庭:
单基因遗传病:如脊髓性肌萎缩症(SMA)、杜氏肌营养不良、血友病等。广东地区常见地贫,通过PGT-M技术已实现100%阻断率。
染色体异常:包括平衡易位、罗氏易位、倒位等结构异常,以及唐氏综合征等非整倍体疾病。反复流产患者中,约50%因胚胎染色体异常导致,PGT-A(非整倍体筛查)技术可将活产率从32%提升至68%。
肿瘤易感基因:如视网膜母细胞瘤、家族性腺瘤性息肉病等,通过PGT技术可生育“无癌宝宝”。
HLA配型需求:已生育重症地贫患儿的家庭,可通过PGT筛选HLA配型胚胎,利用新生儿脐血干细胞救治患病子女。
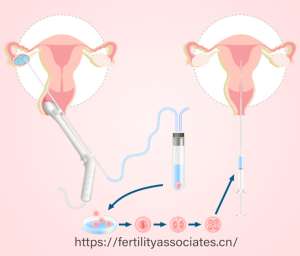
三、操作流程:从检测到移植的全周期管理
遗传咨询:夫妇需接受基因检测,明确致病基因位点及遗传模式。
促排卵与取卵:通过药物刺激卵巢,获取多枚成熟卵子。
体外受精:采用ICSI(单精子注射)技术提高受精率。
胚胎培养与活检:将受精卵培养至囊胚期后取样。
基因检测与筛选:NGS技术可在24小时内完成检测,准确率超99%。
胚胎移植:选择健康胚胎移植,移植后通过HCG检测及B超确认妊娠。
四、实战案例:技术突破下的生命奇迹
案例1:珠海某家庭因携带脊髓性肌萎缩症基因,连续两胎患重症。通过PGT-M技术筛选出健康胚胎,成功生育无病宝宝。
案例2:42岁女性因反复流产求诊,胚胎染色体异常率达80%。通过PGT-A技术筛选整倍体胚胎,单周期活产率提升至18%。
案例3:地贫患儿家庭通过HLA配型PGT技术,生育“救命宝宝”,利用其脐血干细胞完成姐姐的造血干细胞移植。
五、风险与伦理:科学决策的边界
尽管PGT技术可显著降低遗传风险,但仍需关注:
技术局限性:仅能检测已知致病基因,对未知突变或表观遗传异常无效。
胚胎损耗风险:约10%-15%的胚胎因无法发育到囊胚期或检测异常被淘汰。
伦理争议:需严格遵守《人类辅助生殖技术规范》,禁止非医学需要的性别选择。
结语:从“风险生育”到“优生优育”的跨越
三代试管PGT技术通过基因层面的精准干预,为遗传病家庭提供了“零风险”生育的可能。随着NGS技术成本下降及国产化设备普及,单周期费用有望降低50%,技术普及率将持续提升。对于遗传病家庭而言,PGT不仅是生育选择,更是对下一代生命质量的郑重承诺。